Молекулярные механизмы действия ДИМ и его клиническое применение

Молекулярные механизмы действия ДИМ и его клиническое применение
Е.А. Никитина1,2,3, С. В. Орлова1,2, Т. Т. Батышева1,2, Н. В. Балашова1,3,4, М. В. Алексеева1,2, А. Н. Водолазкая5, Е. В. Прокопенко6, Х. А. Магомедова7
1 ФГАОУ ВО «Российский университет дружбы народов» имени Патриса Лумумбы» (РУДН), Москва, Россия
2 ГБУЗ «Научно-практический центр детской психоневрологии Департамента здравоохранения г. Москвы», Россия
3 ФГБУ «Национальный медицинский исследовательский центр терапии и профилактической медицины» Минздрава России, Москва, Россия
4 ГБУЗ МО «Московский областной научно-исследовательский клинический институт имени М. Ф. Владимирского»,Москва, Россия
5 Австрийская клиника микронутриентной терапии Biogena, Москва, Россия
6 ООО «ИНВИТРО», Москва, Россия
7 ООО «Такем энд Ко», Москва, Россия
РЕЗЮМЕ
Оптимальное питание предусматривает необходимость и обязательность полного обеспечения потребностей организма не только в энергии, макро- и микронутриентах, но и в минорных биологически активных веществах. Одними из наиболее перспективных хемопротекторов являются глюкозинолаты и их активные производные, такие как 3,3’-дииндолилметан (ДИМ). ДИМ обладает способностью тормозить развитие и прогрессирование неоплазии за счет регуляции множества внутриклеточных сигнальных путей. В настоящее время проводится изучение клинической эффективности ДИМ при раке молочной железы и простаты, а также исследуется возможность применения антиоксидантных и противовоспалительных свойств ДИМ при нейродегенеративных, метаболических и иммунных заболеваниях.
КЛЮЧЕВЫЕ СЛОВА: 3,3’-дииндолилметан (ДИМ), рак молочной железы, рак простаты, хемопротекция.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы заявляют об отсутствии конфликта интересов.
Публикация выполнена при поддержке Программы стратегического академического лидерства РУДН.
Molecular mechanisms of action of DIM and its clinical application
E. A. Nikitina1,2,3, S. V. Orlova1,2, T. T. Batysheva1,2, N. V. Balashova1,3,4, M. V. Alekseeva1,2, A. N. Vodolazkaya5, E. V. Prokopenko6, Kh. A. Magomedova7
1 Peoples’ Friendship University of Russia named after Patrice Lumumba, Moscow, Russia
2 Scientific and Practical Center for Pediatric Psychoneurology of the Moscow Department of Health, Moscow, Russia
3 National Medical Research Center for Therapy and Preventive Medicine, Moscow, Russia
4 MONIKI M. F. Vladimirskii Moscow Regional Scientific Research Institute, Moscow, Russia
5 Austrian Clinic of Micronutrient Therapy Biogena, Moscow, Russia
6 INVITRO LLC, Moscow, Russia
7 Ltd Takem & Co, Moscow, Russia
SUMMARY
Optimal nutrition requires complete provision of the human needs not only for energy, macro- and micronutrients, but also for minor biologically active substances. Some of the most promising chemoprotectors are lucosinolates and their active derivatives, such as 3,3’-diindolylmethane (DIM). DIM has the ability to inhibit the development and progression of neoplasia by regulating multiple intracellular signaling pathways. Currently, the clinical efficacy of DIM is being studied in breast and prostate cancer, and the possibility of using DIM’s antioxidant and anti-inflammatory properties in neurodegenerative, metabolic and immune diseases is being investigated.
KEYWORDS: 3,3’-diindolylmethane (DIM), breast cancer, prostate cancer, chemoprotection.
CONFLICT OF INTEREST. The authors declare no conflict of interest.
The publication was supported by the RUDN Strategic Academic Leadership Program.
Введение
Хронические неинфекционные заболевания (НИЗ) являются основной причиной смерти населения планеты, они составляют 74 % всех случаев смерти в мире. Каждый год от НИЗ умирает 41 млн человек, в том числе 17 млн не достигших 70 лет. 80 % всех случаев преждевременной смерти приходится на сердечно-сосудистые, онкологические, хронические респираторные заболевания и сахарный диабет [1]. В Российской Федерации сильнее всего растет заболеваемость злокачественными новообразованиями: с 2010 по 2022 г. она выросла с 361,8 до 425,9 на 100 тыс. населения. При этом особенно сильно прогрессировала онкологическая заболеваемость у женщин: с 363,1 до 500,7 на 100 тыс. Самой распространенной формой новообразований у женщин является рак молочной железы (РМЖ). В 2022 г. РМЖ был диагностирован у 2,3 млн женщин и вызвал 670 000 случаев смерти во всем мире [2]. Заболеваемость РМЖ в Российской Федерации выросла за 12 лет с 74,5 до 112,1 на 100 тыс. женщин [3].
В развитии, прогрессировании и осложнении НИЗ, включая онкологические заболевания, одну из ключевых ролей играет несбалансированное питание. Правильное питание предполагает не только адекватный и сбалансированный по калорийности и содержанию макро- и микронутриентов состав, но и обязательное присутствие в рационе минорных* биологически активных веществ.
* Минорные вещества – это такие природные вещества с установленными химической структурой и физиологическим действием, которые присутствуют в пище в малых количествах и играют доказанную роль в поддержании здоровья, а также выступают в качестве экзогенных регуляторов метаболизма [4]. Несмотря на то что минорные вещества содержатся в рационе в количестве нескольких милли- или микрограммов, они чрезвычайно важны для оптимального функционирования организма и хорошей адаптации к изменяющимся условиям окружающей среды. К минорным биологическиактивным веществам относятся инозит, кофеин, коэнзим Q10, липоевая кислота, фенольные соединения и т. п.
Известно, что отдельные минорные вещества и продукты, их содержащие, снижают риск развития или смерти от таких хронических заболеваний, как ишемическая болезнь сердца [5], артериальная гипертензия [6, 7], сахарный диабет [8], отдельные новообразования и др. [9–12]. В случае недостаточного содержания в натуральных продуктах минорные вещества могут дополнительно вводиться в рацион в форме БАД к пище и также будут оказывать адаптогенное и профилактическое действие [13–17].
В то время как воздействие на организм человека таких минорных веществ, как куркумин, расвератрол или полифенолы зеленого чая, хорошо изучено, действие других активно исследуется в настоящее время. К этой группе относятся производные глюкозинолатов, содержащихся в крестоцветных овощах. Из более чем 130 глюкозинолатов особого внимания заслуживает глюкобрассицин, являющийся предшественником биологически активных индольных соединений. В исследовании EPIC-Heidelberg было показано, что женщины потребляют с пищей в среднем 14,8±1,3 мг/д глюкозинолатов, из которыхглюкобрассицин составляет 4,2±0,4 мг [18].
Лучшими источниками глюкобрассицина являются брюссельская, савойская и цветная капуста. В то время как такие крестоцветные, как репа или брюква, будучи хорошими источниками глюкозинолатов в целом, содержат мало глюкобрассицина.
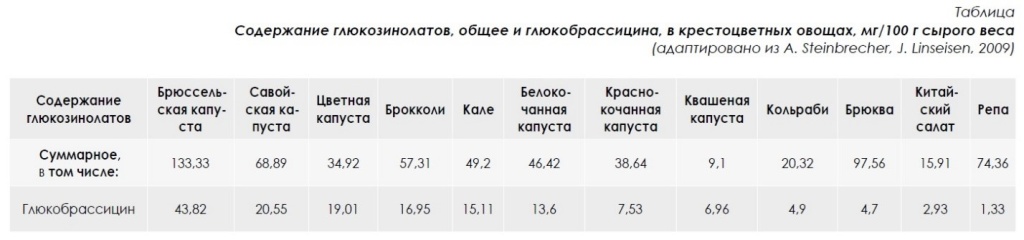
Фермент мирозиназа, высвобождающийся из растительных клеток при измельчении пищи или синтезируемый некоторыми кишечными бактериями, гидролизует глюкобрассицин до нестабильного индол‑3-метилизотиоцианата, который спонтанно распадается с образованием индол‑3-ацетонитрила и индол‑3-карбинола (И3К). Выход И3К из глюкобрассицина составляет около 20 %, что соответствует 0,11–0,18 мг/г сухого веса для брюссельской капусты. Для стимуляции ферментов метаболизма ксенобиотиков взрослым рекомендуется потреблять 50 мг И3К в сутки [4], однако фактическое потребление в западных странах значительно ниже. По оценкам, ежедневное потребление ИЗК из пищи составляет менее 2,6 мг в США и 0,1 мг/кг массы тела в Великобритании [19]. Основным крестоцветным растением в рационе молодых россиян является белокочанная капуста, при этом 44 % опрошенных не включают капустные в ежедневный рацион питания [20].
При низком рН И3К подвергается конденсации, образуя смесь 3,3’-дииндолилметана (ДИМ) с линейными и циклическими тримерами и тетрамерами. ДИМ является основным продуктом, образующимся в кислых условиях как in vitro, так и in vivo в желудке. Активность И3К обусловлена в основном действием ДИМ и заметно снижается, если И3К вводится в обход желудка, например, внутривенно [21, 22].
И3К обладает высокой степенью реактивности и нестабилен в организме, что может создавать трудности при использовании. ДИМ более стабилен, менее реактивен и лучше всего изучен при применении в качестве БАД к пище [23].
В Калифорнийском университете в Беркли было показано, что ДИМ является модулятором врожденной иммунной системы [23]. Учитывая множество положительных эффектов, свойственных ДИМ (рис. 1), Национальный институт рака начал клинические исследования ДИМ при различных формах новообразований. В настоящее время исследуется клиническое действие ДИМ в отношении неоплазии шейки матки, рака молочной железы, простаты и др.
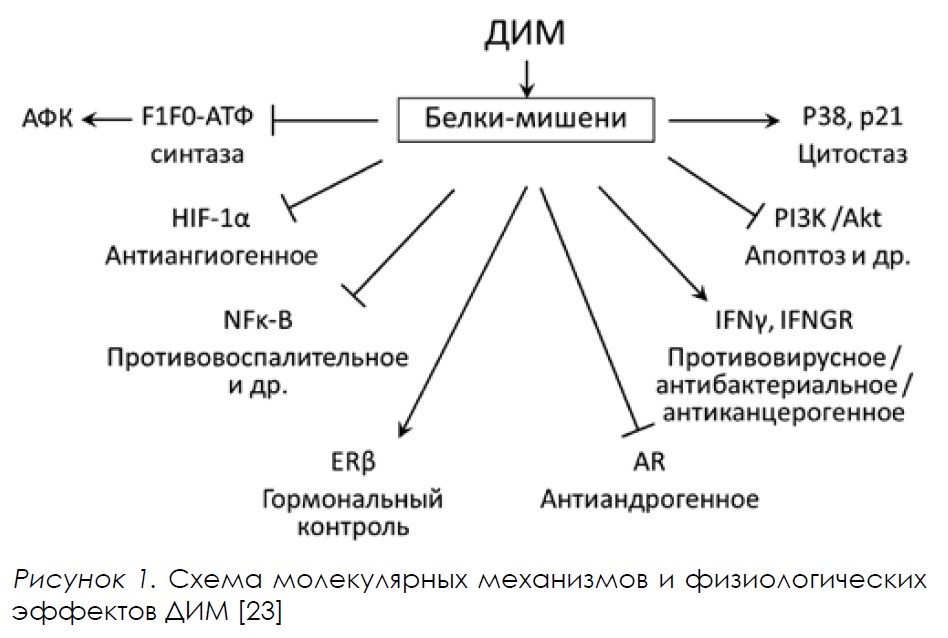
Помимо прямого влияния на определенные молекулы, ДИМ способен регулировать экспрессию генов путем модуляции ДНК-метилтрансфераз, гистондеацетилаз, miРНК, lncRNA и некоторых факторов транскрипции, таких как арильный углеводородный рецептор (AhR), эстрогеновые (ER) и андрогенные рецепторы (AR) и ядерный фактор kB (NF-kB). Например, ингибирование ДНК-метилтрансферазы под действием ДИМ приводило к более низкой экспрессии онкогенов и увеличению генов-супрессоров опухолей. Этот механизм был выявлен в ходе экспериментов на животных моделях, а также на клетках предстательной железы человека, как здоровых, так и раковых [24].
Антиканцерогенное действие
Канцерогенез состоит из ряда последовательных стадий: инициации, размножения опухолевых клеток (промоции) и опухолевой прогрессии. При этом отличительными признаками злокачественных новообразований являются самодостаточность в отношении ростовых сигналов, нечувствительность к рост-ингибиторным сигналам, уклонение от программированной клеточной смерти (апоптоза), неограниченность репликативного потенциала, ангиогенез, тканевая инвазия и метастазирование. В основе развития отдельных опухолей, таких как РМЖ и рак простаты, лежат генетические и экологические факторы, в то время как гормоны, эндо- и экзогенные, играют важную роль в патогенезе и прогрессировании заболевания. В настоящее время большое внимание уделяется также микробиоте, оказывающей гормономодулирующее, иммунорегулирующее и противовоспалительное действие.
ДИМ продемонстрировал способность влиять на множество патологических механизмов на всех стадиях канцерогенеза при раке молочной железы, простаты, легких, толстой кишки, кожи, шейки матки и др.
ДИМ тормозит инициацию канцерогенеза за счет стимуляции механизмов детоксикации в клетках. Он модулирует AhR в цитоплазме, который при транспортировке в ядро активирует транскрипцию генов, стимулирующих экспрессию ферментов детоксикации, включая семейство цитохрома P450 (CYP) I фазы. За счет влияния на AhR можно также усиливать или ослаблять воспаление. Модуляция AhR под действием ДИМ также приводит к активации II фазы детоксикации, опосредованной через Nrf2, которая усиливает выведение генотоксинов и вызывает мощный антиоксидантный ответ. Благодаря активации сигнальных путей AhR и Nrf2 ДИМ усиливает детоксикацию и снижает воспалительную сигнализацию, блокируя потенциальные инициаторы канцерогенеза [25].
Апоптоз
При ксенотрансплантации опухоли толстой кишки человека пероральное введение ДИМ подавляло рост опухоли у мышей. В культуре клеток гепатоцеллюлярной карциномы и злокачественной меланомы ДИМподавлял рост за счет стимуляции митохондриального апоптоза, опосредованного стрессом эндоплазматического ретикулума и индукцией PTEN/Akt соответственно. Ранее было показано, что ДИМ вызывает апоптоз в клетках рака толстой кишки за счет активации каспазы‑8. Еще одним механизмом, лежащим в основе проапоптотического действия ДИМ в клетках колоректального рака человека, является индукция экспрессии активирующего фактора транскрипции 3 (ATF3), опосредованная ATF4.
Остановка клеточного цикла
Комплекс ДИМ и И3К приводил к повышению или понижению экспрессии определенных miRNA и напрямую снижал экспрессию генов, стимулирующих клеточный цикл, таких как CDK4/6 и P27. ДИМ продемонстрировал способность останавливать клеточный цикл в G1 фазе в клетках плоскоклеточного рака пищевода и носоглоточной карциномы. В клетках рака яичников человека ДИМ подавлял рост и деление клеток за счет активации остановки в контрольной точке G2/M. Аналогично в клетках рака толстой кишки человека HT‑29 ДИМ индуцировал остановку как G1, так и G2/M клеточного цикла [25].
Ограничение репликативного потенциала
Известно, что отличительной чертой раковых клеток является безграничный репликативный потенциал, обусловленный сверхэкспрессией теломеразы, поддерживающей длину теломер. В состав теломеразного комплекса входят каталитическая субъединица (теломеразная обратная транскриптаза, hTERT) и теломеразная РНК (hTR), которая содержит матричный участок для синтеза теломерных повторов. В клетках носоглоточной карциномы ДИМ дозозависимо подавлял экспрессию мРНК и белка hTERT, что приводило к значительному снижению активности клеточной теломеразы с последующим укорочением теломер [26]. Необходимо отметить, что ДИМ оказывает влияние на теломеразу не только в раковых, но и в здоровых клетках, что может нести определенные риски. В активированных CD 3/CD 28 мононуклеарных клеткахпериферической крови длительная обработка ДИМ приводила к повреждению ДНК и подавлению пролиферации. Подавление hTERT осуществлялось через сигнальный путь ERα/β-AP1 [27].
Антиангиогенное действие
Накопление индуцируемого гипоксией фактора 1-альфа (HIF‑1α) активирует экспрессию сосудистого эндотелиального фактора роста (VEGF), который, связываясь с рецептором VEGFR на мембранах эндотелиальных клеток, стимулирует пролиферацию, миграцию и прорастание кровеносных сосудов. ДИМ проявляет антиангиогенные свойства. Он снижал содержание HIF‑1α и транскрипционную активностьHIF‑1 в культивируемых в гипоксических условиях клетках рака человека и подавлял ангиогенез в клетках PC 3 рака предстательной железы за счет инактивации mTOR и Akt сигнальных путей [28]. В исследовании ангиогенеза in vivo подкожная инъекция ДИМ ингибировала на 76 % неоваскуляризацию у самок мышей при ксенотрансплантации рака молочной железы [29].
Подавление метастазирования
Метастазирование включает инвазию, деградацию внеклеточного матрикса (ВКМ) и миграцию злокачественных раковых клеток. Инвазия клеток является первым шагом и связана с разрушением механизмов клеточной адгезии, таких как комплекс адгезии E-кадгерина/катенина и фокальная адгезия, опосредованная интегринами. Деградация ВКМ контролируется матриксными металлопротеиназами (ММП) и тканевыми ингибиторами ММП. Контроль за миграцией клеток осуществляется сигнальными системами Rho, Rac или Cdc42. Пероральное введение ДИМ подавляло метастазирование клеток карциномы молочной железы 4T1 в легкие за счет снижения содержания ММП‑2, MMП‑9, тканевого ингибитора металлопротеиназы 1 (ТИМП‑1) и молекул адгезии сосудистых клеток‑1 (VCAM‑1), а также повышения концентрации ТИМП‑2 в сыворотке и легких у мышей линии BALB/c [30]. Аналогичные результаты были получены и на других видах опухолевых клеток (гепатоцеллюлярной карциномы [31, 32], рака простаты [33], плоскоклеточного рака пищевода [34]). ДИМ модулирует активность арил-гидрокарбоновых рецепторов (AHR), благодаря чему ингибируются RhoA/ROCK1 и в последующем ЦОГ2/ПГЕ2 сигнальные пути. В результате удается обратить вспятьпроцесс эпителиально-мезенхимального перехода и ингибировать метастазирование опухоли [34].
Противовоспалительное и антиоксидантное действие
Во множестве экспериментальных моделей было показано, что ДИМ подавляет воспалительную реакцию, вызванную различными факторами [35]. При липополисахарид-индуцированной активации BV2-клеток микроглии ДИМ уменьшал связывание NF-κB с ДНК, в то время как И3К был неактивен. В макрофагальных клетках линии RAW 264.7 ДИМ подавлял ЛПС-стимулированное образование NO, простагландина E 2, ФНО-α, ИЛ‑6 и ИЛ‑1β и ингибировал активность фактора транскрипции AP‑1. В клетках рака предстательной железы человека LNCaP ДИМ значительно подавлял экспрессию белка CCL2 и миграцию клеток THP‑1, обусловленную дигидротестостероном. В модели канцерогенеза кожи, вызванного введением 12-O-тетрадеканоилфорбол‑13-ацетата, ДИМ ослаблял отек уха и подавлял активность ЦОГ‑2, iNOS, хемокинового лиганда 5 мотива CXC и ИЛ‑6, вероятно, за счет подавления активации NF-κB.
В экспериментальных исследованиях было показано, что прием ДИМ повышает концентрацию антиоксидантов (витаминов С и Е, восстановленного глутатиона, СОД, каталазы и глутатионпероксидазы) иснижает концентрацию маркеров окислительного стресса [36].
Отдельные формы рака
Рак молочной железы
В развитии рака молочной железы одну из ключевых ролей играет гормональная регуляция. Метаболизм эстрогенов контролируется системой цитохрома Р‑450, увеличивающего образование 2-гидроксиэстрона (2-ОНЕ1), оказывающего антипролиферативное действие, вместо 16α-гидроксиэстрона (16α-ОНЕ1), оказывающего генотоксическое действие, образующего прочную ковалентную связь с ER и индуцирующего пролонгированный пролиферативный сигнал [37]. Низкое соотношение 2-ОНЕ1/16α-ОНЕ1 является фактором риска эстрогензависимых опухолей, а также цервикальной интраэпителиальной неоплазии.
Клинические исследования показали, что И3К повышает данный коэффициент, однако действие ДИМ на обмен эстрогенов менее однозначно. В исследовании Nikitina D. с соавт. (2015) прием 300 мг/д ДИМ в течение 4–6 недель не оказал статистически значимого влияния на соотношение 2-ОНЕ1/16α-ОНЕ1 (р=0,35) у женщин из группы высокого риска развития РМЖ, носительниц мутации BRCA1 [38]. Аналогичные результаты были показаны в рандомизированном двойном слепом плацебо-контролируемом исследовании у мексиканских женщин в пременопаузальном периоде, имеющих более низкий коэффициент 2-ОНЕ1/16α-ОНЕ1 по сравнению с другими популяциями. Через 30 дней приема 75 мг/д ДИМ соотношение метаболитов ERа в моче увеличивалось, но не достигало статистически значимого результата (p=0,06). При этом у женщин, получавших ДИМ, наблюдалось более выраженное снижение процента жира в организме, чем в группе плацебо (p=0,04) [39]. У женщин 50–70 лет с раком груди в анамнезе прием ДИМ в дозе 108 мг в день в течение 30 дней значительно повышал концентрацию 2-OHE 1 (p=0,020), ДИМ (p=0,045) и кортизола (p=0,039), но незначительно увеличивал соотношение 2-ОНЕ1/16α-ОНЕ1 с 1,46 до 2,14 (p=0,059) [40].
Отсутствие выраженного влияния на метаболизм эстрогенов может быть отчасти объяснено коротким периодом применения ДИМ. Так, в более длительном исследовании (3 менструальных цикла, ~12 недель)комбинация ДИМ с растительными фитонутриентами (декафеинизированным экстрактом зеленого чая, экстрактами куркумы, расторопши, розмарина и др.) приводила к повышению соотношения метаболитов эстрогенов в моче в 4,55 раза [41]. У женщин, получающих тамоксифен по поводу РМЖ, прием ДИМ на протяжении 12 месяцев также приводил к значительному увеличению соотношения 2-ОНЕ1/16α-ОНЕ1 (p<0,001), а также повышению концентрации глобулина, связывающего половые гормоны, по сравнению с плацебо [42].
По данным магнитно-резонансной томографии прием ДИМ в дозе 100 мг/д на протяжении 1 года здоровыми женщинами, носителями мутации BRCA, оказывал положительное влияние на структуру молочныхжелез. Наблюдалось снижение количества фиброзно-железистой ткани (p=0,031) без существенного изменения фонового усиления паренхимы (BPE) (p=0,429), в то время как у женщин, не получавших ДИМ, значимого изменения FGT и BPE за этот период не происходило. Средняя концентрация эстрадиола в группе, получавшей ДИМ, снизилась с 159 до 102 пмоль/л (p=0,01) и тестостерона – с 0,42 до 0,31 пмоль/л(p=0,007), возможно, в результате того, что 78 % женщин были в постменопаузе [43].
Также в настоящее время активно изучается действие ДИМ в отношении профилактики рака шейки матки, вызываемого вирусом папилломы человека высокого канцерогенного риска (ВПЧ ВКР) [44]. Засчет смещения соотношения метаболитов женских половых гормонов ДИМ приводит к торможению развития ВПЧ и уменьшает формирование папилломатозных образований. ДИМ также стимулирует синтез ИФ-γ, транскрипцию рецепторов ИФ-γ и оказывает синергическое действие с ИФ-γ в потенцировании главного комплекса гистосовместимости MHC–I [23, 45].
Рак простаты
ДИМ действует как сильный антагонист андрогенных рецепторов (AR) и напрямую подавляет сигнализацию от АР. ДИМ также избирательно активирует ER-β, которые могут противодействовать действию AR и тем самым влияет на раковые клетки простаты [46]. ДИМ подавляет ядерную транслокацию активированных андрогенных рецепторов.
В исследовании I фазы с повышением дозы ДИМ вводился перорально пациентам с кастрационно-резистентным неметастатическим раком простаты. ДИМ способствовал снижению концентрации ПСА и улучшению эмоционального состояния. Для исследования II фазы было рекомендовано принимать ДИМ в дозе 225 мг дважды в день [47]. Принимаемый в этой дозе ДИМ приводил к повышению содержания ДИМ в ткани простаты. После приема ДИМ в течение 14 дней у 96 % пациентов наблюдалось исчезновение AR из ядра клетки и снижение уровня ПСА у 71 % мужчин. В образцах биопсии простаты, полученных доприема ДИМ, ни у одного пациента не наблюдалось ядерного исключения AR [48].
Взаимодействие с лекарственными препаратами
При рассмотрении возможности применения минорных биологически активных веществ для оптимизации рациона питания онкологических пациентов чрезвычайно важным является вопрос их совместимости с лекарственной терапией. Известно, что многие фитонутриенты (бергамоттин, куркумин, гиперфорин и т. д.), будучи сами по себе хорошими антиоксидантами и онкопротекторами, могут изменять метаболизм химиопрепаратов, снижая их эффективность [49, 50]. Так, сочетанный прием тамоксифена с куркумином приводил к снижению AUC 24 тамоксифена и его активного метаболита эндоксифена у пациенток с раком молочной железы. Предполагают, что прием куркумина (±пиперин) может снизить концентрацию эндоксифена ниже порога эффективности у 20–40 % пациенток [51].
ДИМ оказывает положительное влияние на гормональный обмен, воспаление и свободнорадикальное окисление, но практически не влияет на метаболизм лекарственных средств. Напротив, он дополняет действие лекарственных химиотерапевтических препаратов: так, он усиливает действие паклитаксела в отношении апоптоза клеток. В настоящее время изучают возможность применения ДИМ в качестве средства для снижения устойчивости пациентов к паклитакселу как одному из наиболее часто применяемых противоопухолевых средств [23].
При исследовании действия глюкозинолатов на обмен тамоксифена было показано, что в отличие от И3К ДИМ, применяемый в двух разных дозах в течение 4 дней, не влияет на метаболизм лекарственного препарата в печени крыс [52]. В клиническом исследовании на фоне приема ДИМ содержание тамоксифена в плазме достоверно не снижалось (p=0,06), однако отмечалось снижение концентрации метаболитов тамоксифена, в т. ч. эндоксифена, по сравнению с плацебо (p<0,001) [42].
Наряду с антиканцерогенным действием изучаются другие эффекты ДИМ. Так, ДИМ показал способность защищать от разрушения костную ткань и увеличивать костную массу при моделировании постменопаузального остеопороза. ДИМ подавляет воспалительную реакцию и оксидативный стресс. Предполагают, что в дальнейшем ДИМ можно будет использовать для снижения риска развития воспалительных заболеваний кишечника, для защиты хрящевой ткани при ревматоидном артрите, а также для профилактики нейродегенеративных процессов в мозге [53, 54]. ДИМ подавляет агрегацию тромбоцитов и воспаление на фоне гипоксии, что чрезвычайно важно для предупреждения сердечно-сосудистых заболеваний [55]. Исследуется иммуномодулирующее действие ДИМ при иммунодефицитных состояниях и инфекционных заболеваниях кожи, таких как угревая сыпь. Показано, что ДИМ проявляет не только иммуномодулирующие свойства, подавляя ЛПС-индуцированное воспаление, но и антимикробные. В настоящее время проводится изучение действия ДИМ в отношении различных вирусных и бактериальных агентов, включая гепатит, грипп и антибиотикорезистентные штаммы бактерий. ДИМ регулирует активность ферментов углеводного обмена, препятствуя избыточному подъему концентрации глюкозы и инсулина и подавляя набор массы тела и образование жировой ткани на фоне высокожировой диеты [56,57]. Учитывая влияние ДИМ на обмен веществ и антиоксидантный статус, превосходящее действие И3К, его можно рассматривать как минорное вещество для профилактики ожирения и сахарного диабета, а также их осложнений [58].
Заключение
Глюкозинолаты крестоцветных являются одной из основных групп минорных биологически активных веществ, регулирующих систему детоксикации ксенобиотиков и клеточных сигнальных систем, защищающих организм человека от развития онкологических заболеваний. В настоящее время внимание исследователей обращено к ДИМ как одному из наиболее активных и при этом стабильных метаболитов. Образующийся из глюкобрассицина ДИМ оказывает разностороннее положительное влияние на организм человека, препятствуя инициации, развитию и прогрессированию опухолевого процесса. В клинических исследованиях изучается действие ДИМ в отношении профилактики и комплексной терапии рака молочной железы и простаты. В целом ДИМ можно считать одним из наиболее перспективных фитонутриентов для повышения адаптационных резервов организма и профилактики хронических НИЗ. Необходимы дальнейшие рандомизированные клинические исследования для определения оптимальных дозировок и продолжительности приема ДИМ.

1. Noncommunicable diseases.WHO. https://www.who.int/news-room/fact-sheets/detail/noncommunicable-diseases.
2. Рак молочной железы. Информационные бюллетени ВОЗ. 13 марта 2024 г. https://www.who.int/ru/news-room/fact-sheets/detail/breast-cancer. Breast cancer. World Health Organization (WHO). 13 March 2024 https://www.who.int/news-room/fact-sheets/detail/breast-cancer.
3. Здравоохранение в России. 2023: Стат. сб. Росстат. М., 2023. 179 с. https://rosstat.gov.ru/storage/mediabank/Zdravoohran‑2023.pdf. Healthcare in Russia. 2023: Statistical Collection/Rosstat. M., 2023. 179 p. https://rosstat.gov.ru/storage/mediabank/Zdravoohran‑2023.pdf
4.Методические рекомендации МР 2.3.1.0253–21 «Нормы физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации», утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека – Главным государственным санитарным врачом Российской Федерации 22.07.2021. https://www.rospotrebnadzor.ru/documents/details.php? ELEMENT_ID=18979. Methodical recommendations MR 2.3.1.0253–21 “Norms of physiological requirements in energy and nutrients of various groups of the population of the Russian Federation”, approved by the Head of the Federal Service for Surveillance on Consumer Rights Protection and Human Wellbeing Chief State Sanitary Physician of the Russian Federation 22.07.2021. (In Russ.). https://www.rospotrebnadzor.ru/documents/details.php? ELEMENT_ID=18979
5. Kim Y, Je Y. Tea consumption and the risks of all-cause, cardiovascular disease, and cancer mortality: a meta-analysis of 38 prospective cohort data sets. Epidemiol Health. 2024 Jun; 21: e2024056. DOI: 10.4178/epih.e2024056
6. Wang K, Li Z, He J. Association of caffeine consumption with all-cause and cause-specific mortality in adult Americans with hypertension. Food Sci Nutr. 2024 Mar 8; 12 (6): 4185–4195. DOI: 10.1002/fsn3.4079
7. Borghi C, Tsioufis K, Agabiti-Rosei E, Burnier M, Cicero AFG, Clement D, Coca A, Desideri G, Grassi G, Lovic D, Lurbe E, Kahan T, Kreutz R, Jelakovic B, Polonia J, Redon J, Van De Borne P, Mancia G. Nutraceuticals and blood pressure control: a European Society of Hypertension position document. J. Hypertens. 2020 May; 38 (5): 799–812. DOI: 10.1097/HJH.0000000000002353
8. Chan KY, Wong MMH, Pang SSH, Lo KKH. Dietary supplementation for gestational diabetes prevention and management: a meta-analysis of randomized controlled trials. Arch Gynecol Obstet. 2021 Jun; 303 (6): 1381–1391. DOI: 10.1007/s00404‑021‑06023‑9
9. Guan R, Van Le Q, Yang H, Zhang D, Gu H, Yang Y, Sonne C, Lam SS, Zhong J, Jianguang Z, Liu R, Peng W. A review of dietary phytochemicals and their relation to oxidative stress and human diseases. Chemosphere. 2021 May; 271: 129499. DOI: 10.1016/j.chemosphere.2020.129499
10. Osadnik T, Goławski M Lewandowski P, Morze J, Osadnik K, Pawlas N, Lejawa M, Jakubiak GK, Mazur A, Schwingschackl L, Gąsior M, Banach M. A network meta-analysis on the comparative effect of nutraceuticals on lipid profile in adults. Pharmacol Res. 2022 Sep; 183: 106402. DOI: 10.1016/j.phrs.2022.106402
11. Rosell M, Fadnes LT. Vegetables, fruits, and berries – a scoping review for Nordic Nutrition Recommendations 2023. Food Nutr Res. 2024 Jan 25; 68. DOI: 10.29219/fnr.v68.10455
12. Rodríguez-Negrete EV, Morales-González Á, Madrigal-Santillán EO, Sánchez-Reyes K, Álvarez-González I, Madrigal-Bujaidar E, Valadez-Vega C, Chamorro-Cevallos G, Garcia-Melo LF, Morales-González JA. Phytochemicals and Their Usefulness in the Maintenance of Health. Plants (Basel). 2024 Feb 15; 13 (4): 523. DOI: 10.3390/plants13040523
13. Sazali S, Badrin S, Norhayati MN, Idris NS. Coenzyme Q10 supplementation for prophylaxis in adult patients with migraine-a meta-analysis. BMJ Open. 2021 Jan 5; 11 (1): e039358. DOI: 10.1136/bmjopen‑2020–039358
14. An P, Wan S, Luo Y, Luo J, Zhang X, Zhou S, Xu T, He J, Mechanick JI, Wu WC, Ren F, Liu S. Micronutrient Supplementation to Reduce Cardiovascular Risk. J. Am. Coll. Cardiol. 2022 Dec 13; 80 (24): 2269–2285. DOI: 10.1016/j.jacc.2022.09.048
15. Moretti C, Bonomi M, Dionese P, Federici S, Fulghesu AM, Giannelli J, Giordano R, Guccione L, Maseroli E, Moghetti P, Mioni R, Pivonello R, Sabbadin C, Scaroni C, Tonacchera M, Verde N, Vignozzi L, Gambineri A. Inositols and female reproduction disorders: a consensus statement from the working group of the Club of the Italian Society of Endocrinology (SIE)-Women’s Endocrinology. J. Endocrinol Invest. 2024 Jul 15. DOI: 10.1007/s40618–024–02363-w
16. Wei P, Liu M, Chen Y, Chen DC. Systematic review of soy isoflavone supplements on osteoporosis in women. Asian Pac J. Trop Med. 2012 Mar; 5 (3): 243–8. DOI: 10.1016/S 1995–7645 (12) 60033‑9
17. Singla RK, Wang X, Gundamaraju R, Joon S, Tsagkaris C, Behzad S, Khan J, Gautam R, Goyal R, Rakmai J, Dubey AK, Simal-Gandara J, Shen B. Natural products derived from medicinal plants and microbes might act as a game-changer in breast cancer: a comprehensive review of preclinical and clinical studies. Crit Rev Food Sci Nutr. 2023 Nov; 63 (33): 11880–11924. DOI: 10.1080/10408398.2022.2097196
18. Steinbrecher A, Linseisen J. Dietary intake of individual glucosinolates in participants of the EPIC-Heidelberg cohort study. Ann Nutr Metab. 2009; 54 (2): 87–96. DOI: 10.1159/000209266
19. Reyes-Hernández OD, Figueroa-González G, Quintas-Granados LI, Gutiérrez-Ruíz SC, Hernández-Parra H, Romero-Montero A, Del Prado-Audelo ML, Bernal-Chavez SA, Cortés H, Peña-Corona SI, Kiyekbayeva L, Ateşşahin DA, Goloshvili T, Leyva-Gómez G, Sharifi-Rad J. 3,3’-Diindolylmethane and indole‑3-carbinol: potential therapeutic molecules for cancer chemoprevention and treatment via regulating cellular signaling pathways.Cancer Cell Int. 2023 Aug 26; 23 (1): 180. DOI: 10.1186/s12935‑023‑03031‑4
20. Денисова Е. Л., Королев А. А., Никитенко Е. И., Кирпиченкова Е. В., Фетисов Р. Н., Козлов В. В., Онищенко Г. Г. Гигиеническая оценка содержания индолов в рационе студентов медицинского университета. Вопр. питания. 2018. Т. 87, № 6. С. 22–27. DOI: 10.24411/00 42–88 33‑2018‑10063 https://pubmed.ncbi.nlm.nih.gov/30763487 Denisova E. L., Korolev A. A., Nikitenko E. I., Kirpichenkova E. V., Fetisov R. N., Kozlov V. V., Onishchenko G. G. Hygienic assessment of indoles in the diet of medical students. Voprosy pitaniia [Problems of Nutrition]. 2018; 87 (6): 22–7. DOI: 10.24411/0042‑8833‑2018‑10063 (in Russ.) Available at: https://pubmed.ncbi.nlm.nih.gov/30763487
21. Ramakrishna K, Jain SK, Krishnamurthy S. Pharmacokinetic and Pharmacodynamic Properties of Indole‑3-carbinol in experimental focal ischemic Injury. Eur. J. Drug Metab Pharmacokinet. 2022 DOI: 10.1007/s13318–022–00771-y
22. Williams DE. Indoles Derived From Glucobrassicin: Cancer Chemoprevention by Indole‑3-Carbinol and 3,3’-Diindolylmethane. Front Nutr. 2021 Oct 1; 8: 734334. DOI: 10.3389/fnut.2021.734334
23. Diindolylmethane (DIM) Information Resource Center. An Initiative of Faculty Members and Research Fellows at the University of California at Berkeley https://www.diindolylmethane-dim.com/references.htm
24. Centofanti F, Buono A, Verboni M, Tomino C, Lucarini S, Duranti A, Pandolfi PP, Novelli G. Synthetic Methodologies and Therapeutic Potential of Indole‑3-Carbinol (I3C) and Its Derivatives. Pharmaceuticals (Basel). 2023 Feb 5; 16 (2): 240. DOI: 10.3390/ph16020240
25. Thomson CA, Ho E, Strom MB. Chemopreventive properties of 3,3’-diindolylmethane in breast cancer: evidence from experimental and human studies. Nutr Rev. 2016 Jul; 74 (7): 432–43. DOI: 10.1093/nutrit/nuw010
26. Li F, Xu Y, Chen C, Chen SM, Xiao BK, Tao ZZ. Pro-apoptotic and anti-proliferative effects of 3,3’-diindolylmethane in nasopharyngeal carcinoma cells via downregulation of telomerase activity. Mol Med Rep. 2015 Sep; 12 (3): 3815–3820. DOI: 10.3892/mmr.2015.3836
27. Herz C, Tran HTT, Landerer S, Gaus J, Schlotz N, Lehr L, Schäfer WR, Treeck O, Odongo GA, Skatchkov I, Lamy E. Normal human immune cells are sensitive to telomerase inhibition by Brassica-derived 3,3-diindolylmethane, partly mediated via ERα/β-AP1 signaling. Mol Nutr Food Res. 2017 Sep; 61 (9). DOI: 10.1002/mnfr.201600524
28. Kong D, Banerjee S, Huang W, Li Y, Wang Z, Kim HR, Sarkar FH. Mammalian target of rapamycin repression by 3,3’-diindolylmethane inhibits invasion and angiogenesis in platelet-derived growth factor-D-overexpressing PC 3 cells. Cancer Res. 2008 Mar 15; 68 (6): 1927–34. DOI: 10.1158/0008–5472.CAN‑07–3241
29. Chang X, Tou JC, Hong C, Kim HA, Riby JE, Firestone GL, Bjeldanes LF. 3,3’-Diindolylmethane inhibits angiogenesis and the growth of transplantable human breast carcinoma in athymic mice. Carcinogenesis. 2005 Apr; 26 (4): 771–8. DOI: 10.1093/carcin/bgi018
30. Kim EJ, Shin M, Park H, Hong JE, Shin HK, Kim J, Kwon DY, Park JH. Oral administration of 3,3’-diindolylmethane inhibits lung metastasis of 4T1 murine mammary carcinomacells in BALB/c mice. J. Nutr. 2009 Dec; 139 (12): 2373–9. DOI: 10.3945/jn.109.111864.
31. Li WX, Chen LP, Sun MY, Li JT, Liu HZ, Zhu W. 3’3-Diindolylmethane inhibits migration, invasion and metastasis of hepatocellular carcinoma by suppressing FAK signaling. Oncotarget. 2015 Sep 15; 6 (27): 23776–92. DOI: 10.18632/oncotarget.4196
32. Munakarmi S, Shrestha J, Shin HB, Lee GH, Jeong YJ. 3,3’-Diindolylmethane Suppresses the Growth of Hepatocellular Carcinoma by Regulating Its Invasion, Migration, and ER Stress-Mediated Mitochondrial Apoptosis. Cells. 2021 May 12; 10 (5): 1178. DOI: 10.3390/cells10051178
33. Tsao CW, Li JS, Lin YW, Wu ST, Cha TL, Liu CY. Regulation of carcinogenesis and mediation through Wnt/β-catenin signaling by 3,3’-diindolylmethane in an enzalutamide-resistant prostate cancer cell line. Sci Rep. 2021 Jan 13; 11 (1): 1239. DOI: 10.1038/s41598‑020‑80519‑3
34. Zhu P, Yu H, Zhou K, Bai Y, Qi R, Zhang S. 3,3’-Diindolylmethane modulates aryl hydrocarbon receptor of esophageal squamous cell carcinoma to reverse epithelial-mesenchymal transition through repressing RhoA/ROCK1-mediated COX2/PGE 2 pathway. J Exp Clin Cancer Res. 2020 Jun 16;39(1):113. DOI: 10.1186/s13046–020–01618–7.)
35. Amarakoon D, Lee WJ, Tamia G, Lee SH. Indole‑3-Carbinol: Occurrence, Health-Beneficial Properties, and Cellular/Molecular Mechanisms. Annu Rev Food Sci Technol. 2023 Mar 27; 14: 347–366. DOI: 10.1146/annurev-food‑060721–025531
36. Jayakumar P, Pugalendi KV, Sankaran M. Attenuation of hyperglycemia-mediated oxidative stress by indole‑3-carbinol and its metabolite 3, 3’- Diindolylmethane in C 57BL/6J mice. J. Physiol Biochem. 2014 Jun; 70(2): 525–34. DOI: 10.1007/ s13105‑014‑0332‑5
37.Опыт применения индинола при папилломавирусной инфекции: сб. статей. – М.,2011. – 50 с. https://indinol.ru/assets/files/Sbornik_VPH_A4_out.pdf Experience in theuse of indinol in papillomavirus infection: Sat. articles. Мoscow, 2011. 50 pp.(In Russ.). Available at:https://indinol.ru/assets/files/Sbornik_VPH_A4_out.pdf
38. Nikitina D, Llacuachaqui M, Sepkovic D, Bradlow HL, Narod SA, Kotsopoulos J. The effect of oral 3,3’-diindolylmethane supplementation on the 2:16α-OHE ratio in BRCA1 mutation carriers. Fam Cancer. 2015 Jun; 14 (2): 281–6. DOI: 10.1007/s10689‑015‑9783‑2
39. Godínez-Martínez E, Santillán R, Sámano R, Chico-Barba G, Tolentino MC, Hernández-Pineda J. Effectiveness of 3,3’-Diindolylmethane Supplements on Favoring the Benign Estrogen Metabolism Pathway and Decreasing Body Fat in Premenopausal Women. Nutr Cancer. 2023; 75 (2): 510–519. DOI: 10.1080/01635581.2022.2123535
40. Dalessandri KM, Firestone GL, Fitch MD, Bradlow HL, Bjeldanes LF. Pilot study: effect of 3,3’-diindolylmethane supplements on urinary hormone metabolites in postmenopausal women with a history of early-stage breast cancer. Nutr Cancer. 2004; 50 (2): 161–7. DOI: 10.1207/s15327914nc5002_5
41. Green T, See J, Schauch M, Reil J, Glover M, Brix J, Gerry A, Li K, Newman M, Gahler RJ, Wood S. A randomized, double-blind, placebo-controlled, cross-over trial to evaluate the effect of EstroSense® on 2-hydroxyestrone:16α-hydroxyestrone ratio in premenopausal women. J. Complement Integr Med. 2022 Oct 6; 20 (1): 199–206. DOI: 10.1515/jcim‑2022–0301
42. Thomson CA, Chow HHS, Wertheim BC, Roe DJ, Stopeck A, Maskarinec G, Altbach M, Chalasani P, Huang C, Strom MB, Galons JP, Thompson PA. A randomized, placebo-controlled trial of diindolylmethane for breast cancer biomarker modulation in patients taking tamoxifen. Breast Cancer Res Treat. 2017 Aug; 165 (1): 97–107. DOI: 10.1007/s10549‑017‑4292‑7
43. Yerushalmi R, Bargil S, Ber Y, Ozlavo R, Sivan T, Rapson Y, Pomerantz A, Tsoref D, Sharon E, Caspi O, Grubsrein A, Margel D. 3,3-Diindolylmethane (DIM): a nutritional intervention and its impact on breast density in healthy BRCA carriers. A prospective clinical trial. Carcinogenesis. 2020 Oct 15; 41 (10): 1395–1401. DOI: 10.1093/carcin/bgaa050
44. Сайт «Международная ассоциация по патологии шейки матки и кольпоскопии». URL: https://ifcpc.org/ the International Federation of colposcopy and cervicalpathology. https://ifcpc.org
45. Xue L, Pestka JJ, Li M, Firestone GL, Bjeldanes LF. 3,3’-Diindolylmethane stimulates murine immune function in vitro and in vivo. J. Nutr Biochem. 2008 May; 19 (5): 336–44. DOI: 10.1016/j.jnutbio.2007.05.004
46. Verma V, Sharma V, Singh V, Sharma S, Bishnoi AK, Chandra V, Maikhuri JP, Dwivedi A, Kumar A, Gupta G. Designed modulation of sex steroid signaling inhibits telomerase activity and proliferation of human prostate cancer cells. Toxicol Appl Pharmacol. 2014 Oct 15; 280 (2): 323–34. DOI: 10.1016/j.taap.2014.08.002
47. Heath EI, Heilbrun LK, Li J, Vaishampayan U, Harper F, Pemberton P, Sarkar FH. A phase I dose-escalation study of oral BR-DIM (BioResponse 3,3’- Diindolylmethane) in castrate-resistant, non-metastatic prostate cancer. Am. J. Transl Res. 2010 Jul 23; 2 (4): 402–11. PMID: 20733950; PMCID: PMC 2923864. https://pubmed.ncbi.nlm.nih.gov/20733950
48. Hwang C, Sethi S, Heilbrun LK, Gupta NS, Chitale DA, Sakr WA, Menon M, Peabody JO, Smith DW, Sarkar FH, Heath EI. Anti-androgenic activity of absorption-enhanced 3, 3’-diindolylmethane in prostatectomy patients. Am. J. Transl Res. 2016 Jan 15; 8 (1): 166–76. PMID: 27069550; PMCID: PMC 4759426. https://pubmed.ncbi.nlm.nih.gov/27069550
49. Pilla Reddy V, Jo H, Neuhoff S. Food constituent- and herb-drug interactions in oncology: Influence of quantitative modelling on Drug labelling. Br. J. Clin. Pharmacol. 2021 Oct; 87 (10): 3988–4000. DOI:10.1111/bcp.14822
50. Chan WJ, Adiwidjaja J, McLachlan AJ, Boddy AV, Harnett JE. Interactions between natural products and cancer treatments: underlying mechanisms and clinical importance. Cancer Chemother Pharmacol. 2023 Feb; 91 (2): 103–119. DOI: 10.1007/s00280–023–04504-z
51. Hussaarts KGAM, Hurkmans DP, Oomen-de Hoop E, van Harten LJ, Berghuis S, van Alphen RJ, Spierings LEA, van Rossum-Schornagel QC, Vastbinder MB, van Schaik RHN, van Gelder T, Jager A,van Leeuwen RWF, Mathijssen RHJ. Impact of Curcumin (with or without Piperine) on the Pharmacokinetics of Tamoxifen. Cancers (Basel). 2019 Mar 22; 11 (3): 403. DOI: 10.3390/cancers11030403
52. Parkin DR, Malejka-Giganti D. Differences in the hepatic P450-dependent metabolism of estrogen and tamoxifen in response to treatment of rats with 3,3’-diindolylmethane and its parent compound indole‑3-carbinol. Cancer Detect Prev. 2004; 28 (1): 72–9. DOI: 10.1016/j.cdp.2003.11.006
53. Kim HW, Kim J, Kim J, Lee S, Choi BR, Han JS, Lee KW, Lee HJ. 3,3’-Diindolylmethane inhibits lipopolysaccharide-induced microglial hyperactivation and attenuates brain inflammation. Toxicol Sci. 2014 Jan; 137 (1): 158–67. DOI: 10.1093/toxsci/kft240
54. Du H, Zhang X, Zeng Y, Huang X, Chen H, Wang S, Wu J, Li Q, Zhu W, Li H, Liu T, Yu Q, Wu Y, Jie L. A Novel Phytochemical, DIM, Inhibits Proliferation, Migration, Invasion and TNF α Induced Inflammatory Cytokine Production of Synovial Fibroblasts From Rheumatoid Arthritis Patients by Targeting MAPK and AKT/mTOR Signal Pathway. Front Immunol. 2019 Jul 23; 10: 1620. DOI: 10.3389/fimmu.2019.01620
55. Ramakrishna K, Singh N, Krishnamurthy S. Diindolylmethane ameliorates platelet aggregation and thrombosis: In silico, in vitro, and in vivo studies. Eur J Pharmacol. 2022 Mar 15; 919: 174812. DOI: 10.1016/j.ejphar.2022.174812
56. Yang H, Seo SG, Shin SH, Min S, Kang MJ, Yoo R, Kwon JY, Yue S, Kim KH, Cheng JX, Kim JR, Park JS, Kim JH, Park JHY, Lee HJ, Lee KW. 3,3’-Diindolylmethane suppresses high-fat diet-induced obesity through inhibiting adipogenesis of pre-adipocytes by targeting USP2 activity. Mol Nutr Food Res. 2017 Oct; 61 (10). DOI: 10.1002/mnfr.201700119
57. Poornima J, Mirunalini S. Regulation of carbohydrate metabolism by indole‑3-carbinol and its metabolite 3,3’-diindolylmethane in high-fat diet-induced C 57BL/6J mice. Mol Cell Biochem. 2014 Jan; 385 (1–2): 7–15. DOI: 10.1007/s11010‑013‑1808‑2
58. Choi KM, Yoo HS. Amelioration of Hyperglycemia-Induced Nephropathy by 3,3’-Diindolylmethane in Diabetic Mice. Molecules. 2019 Dec 6; 24 (24): 4474. DOI: 10.3390/molecules24244474
Сведения об авторах
Никитина Елена Александровна, к. м. н., доцент кафедры диетологии и клинической нутрициологии1, научный сотрудник2, эксперт Методического аккредитационно-симуляционного центра3. E-mail: nikitina-ea1@rudn.ru. ORCID: 0000‑0003‑3220‑0333
Орлова Светлана Владимировна, д. м. н., проф., зав. кафедрой диетологии и клинической нутрициологии1, главный научный сотрудник2. E-mail: orlova-sv@rudn.ru. ORCID: 0000‑0002‑4689‑3591
Батышева Татьяна Тимофеевна, д. м. н., проф., заслуженный врач РФ, директор2, глав. внештатный детский специалист невролог ДЗМ, глав. внештатный детский специалист по медицинской реабилитации Минздрава России, зав. кафедрой неврологии, физической, реабилитационной медицины и психологии детского возраста1. ORCID: 0000‑0003‑0928‑2131
Балашова Наталья Валерьевна, к. б. н., доцент кафедры диетологии и клинической нутрициологии1, доцент кафедры клинической лабораторной диагностики факультета усовершенствования врачей4. E-mail: BalashovaN 77@mail.ru. SPIN: 2355–6837. Author ID: 832745. ORCID: 0000‑0002‑0548‑3414
Алексеева Марина Валерьевна, к. м. н., зам. директора по организационно-методической работе2. ORCID: 0000‑0001‑8448‑8493
Водолазкая Ангелина Николаевна, врач-диетолог6. E-mail: drvodolazkaya@gmail.com. ORCID: 0000‑0002‑5203‑1082
Прокопенко Елена Валерьевна, врач-эндокринолог, диетолог, руководитель отдела развития и сопровождения медицинских информационных систем и сервисов5. E-mail: elvprokopenko@gmail.com. ORCID: 0000‑0002‑3811‑9459
Магомедова Хадижат Абдулхаликовна, провизор, генеральный директор7. E-mail: hadiga28@mail.ru. ORCID 0000‑0001‑8744‑2976
1 ФГАОУ ВО «Российский университет дружбы народов имени Патриса Лумумбы» (РУДН), Москва, Россия
2 ГБУЗ «Научно-практический центр детской психоневрологии Департамента здравоохранения г. Москвы», Россия
3 ФГБУ «Национальный медицинский исследовательский центр терапии и профилактической медицины» Минздрава России, Москва, Россия
4 ГБУЗ МО «Московский областной научно-исследовательский клинический институт имени М. Ф. Владимирского», Москва, Россия
5 Австрийская клиника микронутриентной терапии Biogena, Москва, Россия
6 ООО «ИНВИТРО», Москва, Россия
7 ООО «Такем энд Ко», Москва, Россия
Автор для переписки: Орлова Светлана Владимировна. E-mail: rudn_nutr@mail.ru
Для цитирования: Никитина Е. А., Орлова С. В., Батышева Т. Т., Балашова Н. В., Алексеева М. В., Водолазкая А. Н., Прокопенко Е. В., Магомедова Х. А. Молекулярные механизмы действия ДИМ и его клиническое применение. Медицинский алфавит. 2024; (19): 9–15. https://doi.org/10.33667/2078‑5631‑2024‑19‑9‑15
About authors
Nikitina Elena A., PhD Med, associate professor at Dept of Dietetics and Clinical Nutrition1, Research Fellow 2, Expert of the Methodological Accreditation and Simulation Center3 E-mail: nikitina-ea1@rudn.ru. ORCID: 0000‑0003‑3220‑0333
Orlova Svetlana V., DM Sci (habil.), professor, head of Dept of Dietetics and Clinical Nutritiology1, Chief Researcher2. E-mail: rudn_nutr@mail.ru. ORCID: 0000‑0002‑4689‑3591
Batysheva Tatyana T., DM Sci (habil.), professor, Honored Doctor of the Russian Federation, director2, chief pediatric neurologist of the Health Dept of the City of Moscow, chief pediatric specialist in medical rehabilitation of the Ministry of Health of the Russian Federation, head of Dept of Neurology, Physical, Rehabilitation Medicine and Psychology of Childhood1. ORCID: 0000‑0003‑0928‑2131
Balashova Natalya V., PhD Bio Sci, assistant professor at Dept of Clinical Laboratory Diagnostics of the Faculty of Advanced Training of Doctors3, assistant professor at Dept of Dietetics and Clinical Nutritiology1. E-mail: BalashovaN 77@mail.ru SPIN: 2355–6837. Author ID: 832745. ORCID: 0000‑0002‑0548‑3414
Alekseeva Marina V., PhD Med, deputy director for Organizational and Methodological Work2. ORCID – 0000‑0001‑8448‑8493
Vodolazkaya Angelina N., dietitian6. E-mail: drvodolazkaya@gmail.com. ORCID: 0000‑0002‑5203‑1082
Prokopenko Elena V., endocrinologist, dietitian5. E-mail: elvprokopenko@gmail.com. ORCID: 0000‑0002‑3811‑9459
Magomedova Khadizhat A., provizor, general director7. E-mail: hadiga28@mail.ru. ORCID 0000‑0001‑8744‑2976
1 Peoples’ Friendship University of Russia named after Patrice Lumumba, Moscow, Russia
2 Scientific and Practical Center for Pediatric Psychoneurology of the Moscow Department of Health, Moscow, Russia
3 National Medical Research Center for Thera py and Preventive Medicine, Moscow, Russia
4 MONIKI M. F. Vladimirskii Moscow Regional Scientific Research Institute, Moscow, Russia
5 Austrian clinic of micronutrient therapy Biogena, Moscow, Russia
6 “INVITRO” Limited Liability Company, Moscow, Russia
7 Ltd Takem & Co, Moscow, Russia
Corresponding author: Orlova Svetlana V. E-mail: rudn_nutr@mail.ru
For citation: Nikitina E. A., Orlova S. V., Batysheva T. T., Balashova N. V., Alekseeva M. V., Vodolazkaya A. N., Prokopenko E. V., Magomedova Kh. A. Molecular mechanisms of action of DIM and its clinical application. Medical alphabet. 2024; (19): 9–15. https://doi.org/10.33667/2078‑5631‑2024‑19‑9‑15




